2020.9.7改定(2013.8.4)
pirika.comで化学
>チャピエモン-3rd Pirika Origin (CPO)
> ハンセン溶解度パラメータ (HSP)
>HSPiP(実践ハンセン溶解度パラメータ)ソフトウエアー
> HSPiPの購入方法
> HSPiPを用いた解析例
>基礎 >応用 >ポリマー >医薬品など >環境・溶媒設計 >分析
>その他 >DIY/YMB >アバターチュートリアル >次世代に向けて
>次世代HSP2技術
> 化学全般
>Pirika Pro ツール群
ブログ
業務案内
お問い合わせ
2025.5.16
「あなたは、酸? 塩基?」オレイン酸の溶解性を次世代のHSP2で解析した。
昔は、アルコールの異常性をクラスターを作ることによるとして、dHの値を変えたものを用意した。でも、今回計算し直してみると、ルイスの酸塩基を持ち込むとメタノールの異常性はなくなると言う結果になった。解釈が広がってきた。
今年の第4回HSP開発者会議(2013, 6月デンマーク)でメタノールの溶解異常性について議論された。
Charles(ハンセン先生)がとても興味深い情報を、古い書籍から示してくださった。
“Macromolecular Solutions: Solvent Property Relationships in Polymer Pergamon Pr (1982/03)”, Raymond Benedict Seymour (著者)
古い本なので入手は困難であろうから、概要だけ簡単に説明しよう。
P166-
Elastomer/Gasoline Blends interaction I. (エラストマーとガソリン混合物の相互作用 1)
メタノールとガソリン混合物のエラストマー上での効果
この章では、フッ素系のエラストマーの各種アルコールに対する防潤性を検討している。
エタノールはたかだか5.4%(体積増加)しか膨潤しないのにメタノールでは100%膨潤する!
そして著者は(186ページ)次のように結論づけている。
”メタノールのHSPとエラストマーのHSPを比べると、最も大きな違いは δHの値である。
このことから考えるに、純粋なメタノールは非常に強く水素結合しており、従って非常に低いδHを持っていると考えざるを得ない。”
そしてメタノールのクラスターとして以下の構造を提案している。
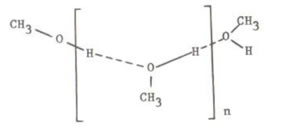
この構造の妥当性を赤外スペクトラムで検証した結果を後に示すとあるが、どこにも無いようである。
このメタノールの異常性をもう少し詳しく見てみよう。
データを提供するので、自分でも確認してみよう。
データをコピーしてエクセルなどにペーストしておこう。
Troutonの通則: 蒸発のエントロピーは様々な液体でほぼ同一の値(85–88 J K−1 mol−1)となる。
蒸発のエントロピーは、蒸発のエンタルピーを沸点の温度で割った値として定義される。(WikiPediaから)
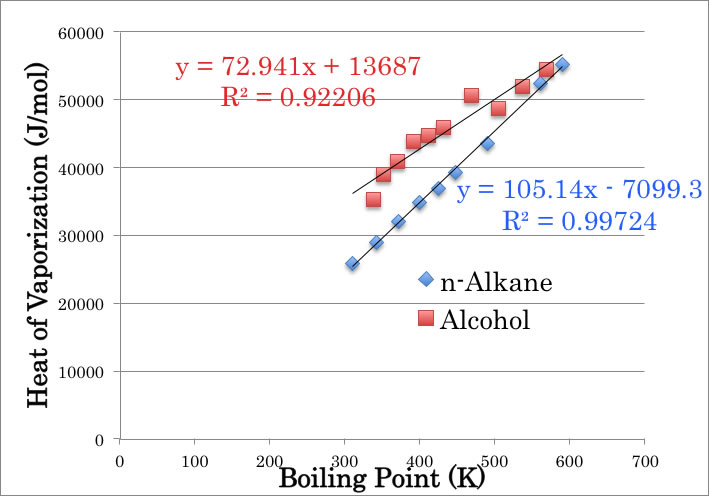
そこで、沸点に対して、沸点における蒸発潜熱をプロットすると上の図のようにきれいな相関が得られる。
赤四角(アルコール群)の一番左端がメタノールである。線から少し外れるがそんなに悪くはない。
Troutonの通則は著名であるのでご存知の方も多いだろうが、次の通則はどれだけ知られているか不明ではある(とりあえず、Pirikaの通則1と呼んでおこう)。
液体の密度から計算される分子体積と25℃での蒸発潜熱をプロットすると下の図に示すように非常にきれいな直線が得られる。
この場合にはメタノールが例外になることもない。
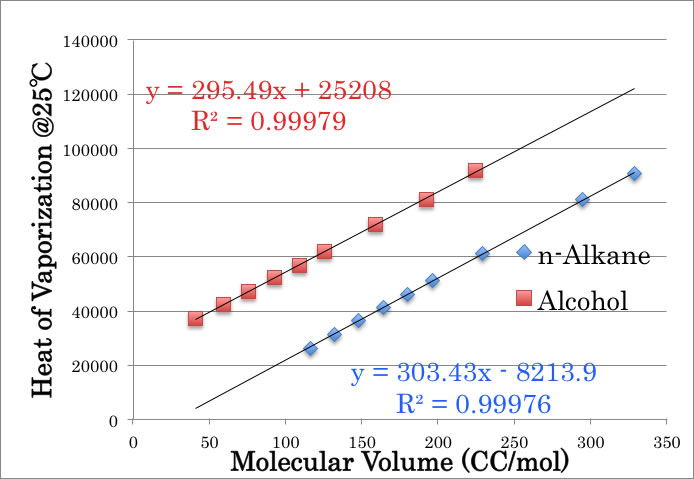
このPirikaの通則1は、ハンセンの溶解度パラメータ(HSP)を使う上ではTroutonの通則よりも利用価値が高い。
それはHSPでは次式に従って全HSP(tot HSP)を計算するからだ。
totHSP= SQRT( (Hv@25 – RT)/Mol Volume)
そこで、Hv@25と分子体積(Mol Volume)は非常に重要な値となる。
これらのものにはメタノールの異常性は見当たらず、従ってHSPiPに搭載されているメタノールのパラメータは正しいと言って間違いない。
もし、最初の書籍の記載のようにメタノールだけが水素結合性の直線的なクラスターを作り、他のアルコールが直線的なクラスターを作らないのならthermo-dynamicな物性値としてはどのような値が変わってくるだろうか?
例えば粘度などは変わってくるように思われる。
これも一般的かどうか知らないが、分子体積のルートと粘度の対数をプロットすると化合物ごとに直線になる(Pirikaの通則2と呼ぶ)。
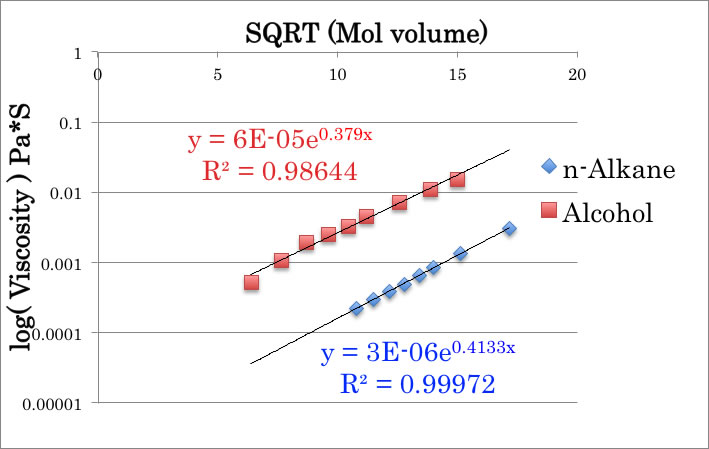
そこで粘度的に考えてもメタノールは異常値であるとは言えないだろう。
現実問題として、メタノールのHSP [14.7, 12.3, 22.3]をn-エイコサンの溶解性に適用してみた結果を下図に示す。
n-エイコサンからのHSP距離が長くなるにつれ溶解性が低下し、メタノール(赤四角)にはほとんど溶解しない。
この結果はメタノールが高いδHを持っていると考えてよい事を示している。
データは次のようになる。
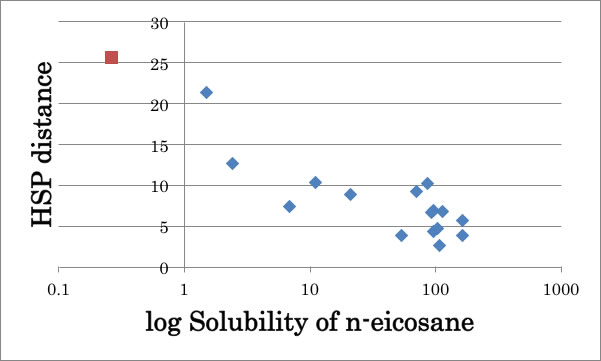
最初の書籍にあったような水素結合による直線的なクラスター(δHが非常に低下)を考える必要は無い。多くのポリマーの溶解性ではエイコサンと同様、δHの低下は考える必要は無い。
ところが、オレイン酸の溶解度を検討した所、アルコール溶媒だけ非常におかしな挙動が見られた。
データは次のようになる。
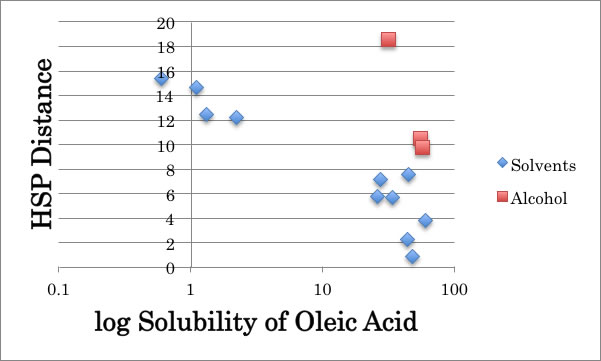
メタノールはHSP距離から考えられるよりも非常に多くのオレイン酸を溶解する。(赤四角の一番左)
そこでこの場合には”クラスターモデル”を導入して考えなくてはならない。
オレイン酸のHSPは [16.0, 2.8, 6.2]であるので、メタノールはクラスターを生成する事によって、δPとδHの両方が小さくならなくてはならない。
クラスターを考える時にメタノールだけから作られるクラスターと、メタノールと溶質の両方からできるクラスターが考えられる。
この二つは区別する事はできない。
クラスターを形成するエネルギーは水素結合から来るのだから、クラスター中に幾つの分子が集まっているかは、メタノールの水素結合力と溶質の水素結合力の兼ね合いで決まる。
そこで、溶質によって異なり、一つには決まらないだろう。
クラスターの形:
Raymond の書籍ではクラスターの形は直線構造とした。
すると何故他のアルコールでは直線のクラスターを取らないのか説明できない。
自分の考えでは、こうした直線構造のクラスターはアルコール化合物に普遍的で、どのアルコール化合物も持ちうる。
(赤外で3200カイザー付近にある広がったバンドがそれに相当するのか?)
そうした直線構造のクラスターは普遍的に存在するとして、蒸発潜熱や粘度についてメタノールは異常ではない。
それではどういうクラスターを作った場合に異常になりうるのだろうか?
また、どのようなクラスターを考えた時にメタノールのみがそのクラスター構造を取りうるのだろうか考えてみよう。
例えばグリコールエーテルを考えてみよう。
CH3OCH2CH2OH [16, 8.2, 15]
CH3OCH2CH2OCH2CH2OH [16.2, 7.8, 12.6]
CH3OCH2CH2OCH2CH2OCH2CH2OH [16.2, 7.6, 12.5]
これがどんどん長くなればPEG(ポリエチレングリコール)になるのだが、ある所まではδPとδHが小さくなるが、オレイン酸ほどまでは低下しない事は明らかだろう。
末端にOHが残るようなクラスターを考えていては駄目であろう。
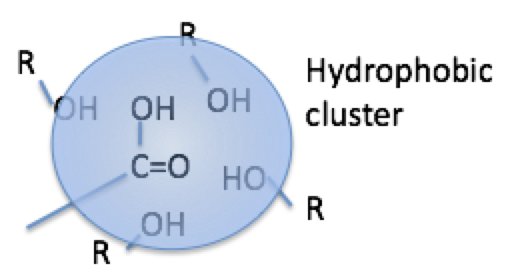
自分は末端水酸基の効果を消すために3次元クラスターを考えた。
試しにメタノールを界面活性剤とした” Water in Oil “のエマルジョンを考えてみよう。
水酸基は大きな表面エネルギーをもつので、オイル中で表面エネルギーを低下させるためメチル基をオイルの側に突き出し、水酸基は内側に凝集し始める。
メタノールという界面活性剤は何分子で一つのクラスターを作るのだろうか?
2分子、ダイマーでは余りに小さいだろう。
オイルは簡単に水素結合部分にアクセスできるだろう。
3量体は平面構造を取るのだろうか?
それにしても平面の上下方向から水素結合部分にアクセスできるだろう。
4量体がピラミッド構造をとり、ピラミッドの各頂点にメチル基を置き、水酸基をピラミッドの内部に置いた場合、オイルから水酸基は全く見えなくなり、末端の水酸基も無くなる。
そのような擬似溶媒のHSPを考えてみよう。
例えばメチル基を4つ持つ構造としては
CH3-O-t-Bu [14.8, 4.3, 5]
CH3-C(=O)-t-Bu [15.3, 6.3, 3]
CH3-COO-tBu [15, 3.7, 6]
などがあるが、これらのHSPは非常にオレイン酸のHSP [16.0, 2.8, 6.2]に近い。
これについては、全く証拠は無いのだが、メタノールのδPとδHをメタノールの会合数3や4で割ってみよう。
Methanol [14.7, 12.3, 22.3]
3-mer [14.7,12.3/3, 22.3/3]=[14.7, 4.1, 7.4]
4-mer [14.7, 12.3/4, 22.3/4]=[14.7,3.1, 5.6]
4量体のHSPはCH3-O-t-BuのHSPと非常に近くなる。
そこでメタノールの最小クラスターはピラミッド構造をとれる4量体であるとする。
(この計算は、電荷平衡法で計算したものだ。各原子上の電荷を計算。を参照してほしい)
この3次元構造に対してQEQを使って電荷を計算した結果も表示される。1分子のメタノールとOHが集まった時とで酸素の電荷がどう変化するか確認して見よう。
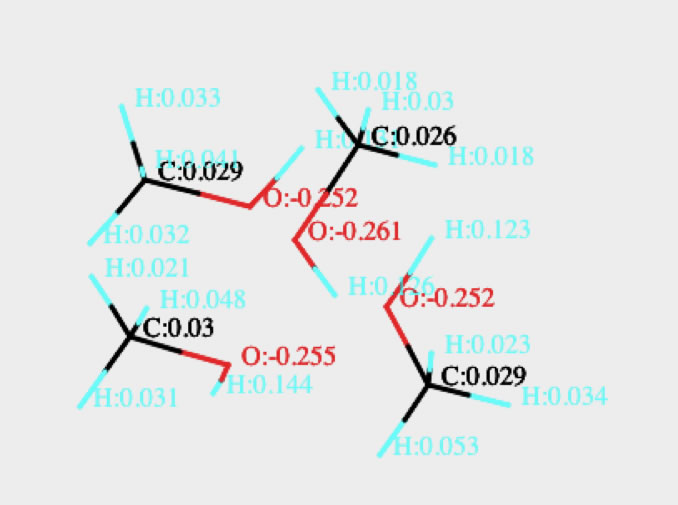
通常のバルクのメタノールは直線構造のクラスターを取るかもしれないが、そのHSPは通常のアルコールのものだ。
フッ素ポリマーのような疎水表面やその内部ではメタノールは表面エネルギーを低下させるためにピラミッド構造を取り始める。
そしてピラミッド構造のHSPはフッ素ポリマーのHSPに近くなりポリマーを強く膨潤させる。
4量体のHSPから計算したHSP距離と(緑色の三角)実溶解度は非常に高い相関がある事が以下の図から明らかであろう。
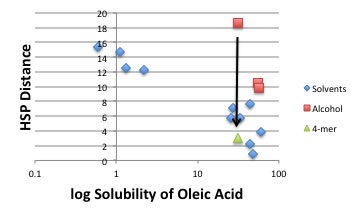
このように、メタノールのHSPは [14.7, 12.3, 22.3] から [14.7,3.1, 5.6] まで、溶質の水素結合エネルギーによって変化する。
ある意味、カメレオン・タイプのHSPであることが明らかになった。
他のより鎖の長いエタノール、プロパノールもピラミッド型のクラスターを作ると考えるかもしれない。
しかし中心の4つの水酸基に対して、鎖の長さが長くなると安定ではいられなくなるのだろう。
結論
1: メタノールがクラスターを作るかどうかは溶質によって異なる。
2: クラスターを作ったとしても、その効果は会合数によって異なる。
非常に曖昧な結論で申し訳ないが、会合性の溶媒で溶解性試験の結果がHSPだけで説明できない事があった場合にはこの結果を思い出して欲しい。 δPとδHの値を 2, 3, 4で割ってみて、どのようなFitになるか試してみてほしい。
言葉としての2量体、3量体、4量体にこだわらないで頂きたい。
特に溶質とメタノールが作るクラスターの場合XX量体というのは意味は無いだろう。
大事なのは一番低い限界が[14.7,3.1, 5.6] まで下がりうるという事だけだ。
自分の経験では、水(メタンハイドレートの系) 、DMSO, DMF そして 1,4-Dioxaneなどの系で3次元クラスタを作り、水素結合効果などが低下するようだ。
またHSP50で発表したように溶媒の蒸発のエネルギーを正則溶媒分のδregとネットワーク用のδnetに分けて考えるのも有効だ。
δtot^2 = δreg^2 + δnet^2δregはTroutonの通則から簡単に求まる。
詳しくは私の発表資料を読んでほしい。
そして、ポリマー中の拡散係数などの物性値に対しても、クラスター構造の違いやHSPの違いが効いてくることだろう。
燃料電池の分野ではフッ素系の膜をメタノールが透過してしまう問題がある。何故、親水性のメタノールがフッ素系の膜を透過してしまうのか?
フッ素系のバイトンのゴムがガソリンとアルコールの混合液に膨潤してしまう。
このようなクラスターを考えると理解が進むかもしれない。
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください
