2011.3.28
pirika.comで化学
>チャピエモン-3rd Pirika Origin (CPO)
> ハンセン溶解度パラメータ (HSP)
> 化学全般
> 情報化学 >物性化学 >高分子化学 >化学工学 >その他の化学 >昔のもの
>Pirika ツール群
ブログ
業務案内
お問い合わせ
>物性化学 > Joback法
[1. 概要]
Lydersenの臨界定数推算は原子団寄与法を使ったものだ。 分子を構成する原子団が決まれば分子の物性は決まる。JOBACK法は原子団寄与法の1つの完成形だ。多くのプロセス・シミュレータに搭載されている。
逆に現在(2026)ではDeep Learningを使えば沸点の推算など簡単にできるだろう。
原子団寄与法という技術自体必要のないものになってしまっている。その分沸点に関する知見は得られなくなる。例えば分子にCH2が1つ増えたら沸点は22.88℃高くなる。化学者のセンスがあればDBに値を登録する時にセンスを働かせることができる。データ値に沸点の場合には°F、℃、°Kの単位がある。他の物性値も単位が異なることもある。
ビッグ・データに単位の異なるデータが混じったときに化学者のセンスは重要になる。
原子団の加算値が求まっていない場合にどのように推算式を構築したかをまとめておく。
[2. Joback法計算方法]
WikipediaのJoback method法のページに原子団のパラメータが与えられている。
| Group | Tc | Pc | Vc | Tb | Tm | Hform | Gform | a | b | c | d | Hfusion | Hvap | ηa | ηb |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Critical-state data | Temperatures of phase transitions | Chemical caloric properties | Ideal-gas heat capacities | Enthalpies of phase transitions | Dynamic viscosity | ||||||||||
| Non-ring groups | |||||||||||||||
| −CH3 | 0.0141 | −0.0012 | 65 | 23.58 | −5.10 | −76.45 | −43.96 | 1.95E+1 | −8.08E−3 | 1.53E−4 | −9.67E−8 | 0.908 | 2.373 | 548.29 | −1.719 |
| −CH2− | 0.0189 | 0.0000 | 56 | 22.88 | 11.27 | −20.64 | 8.42 | −9.09E−1 | 9.50E−2 | −5.44E−5 | 1.19E−8 | 2.590 | 2.226 | 94.16 | −0.199 |
| >CH− | 0.0164 | 0.0020 | 41 | 21.74 | 12.64 | 29.89 | 58.36 | −2.30E+1 | 2.04E−1 | −2.65E−4 | 1.20E−7 | 0.749 | 1.691 | −322.15 | 1.187 |
各物性の計算値は次式で与えられる。
Normal boiling point
![{\displaystyle T_{\text{b}}[{\text{K}}]=198.2+\sum T_{{\text{b}},i}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/815c1bbc824ba86648bf7b031f05897ce8989943)
Melting point
![{\displaystyle T_{\text{m}}[{\text{K}}]=122.5+\sum T_{{\text{m}},i}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6e7c7897d30e60ac8295a683763edd0e6ca58bcd)
Critical temperature
![{\displaystyle T_{\text{c}}[{\text{K}}]=T_{\text{b}}\left[0.584+0.965\sum T_{{\text{c}},i}-\left(\sum T_{{\text{c}},i}\right)^{2}\right]^{-1}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/23d758beed83705bd6b329f3d256b106e0a6a34c)
Critical pressure
![{\displaystyle P_{\text{c}}[{\text{bar}}]=\left[0.113+0.0032\,N_{\text{a}}-\sum P_{{\text{c}},i}\right]^{-2},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/85925f3f1489f0f5550018673c083de4449d0f24)
Critical volume
![{\displaystyle V_{\text{c}}[{\text{cm}}^{3}/{\text{mol}}]=17.5+\sum V_{{\text{c}},i}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f6cd4837150b1524a1968d7508a93289fc6d3133)
Heat of formation (ideal gas, 298 K)
![{\displaystyle H_{\text{formation}}[{\text{kJ}}/{\text{mol}}]=68.29+\sum H_{{\text{form}},i}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8ff4df9e7e76e9ed5d5635acf868cbb74e700b89)
Gibbs energy of formation (ideal gas, 298 K)
![{\displaystyle G_{\text{formation}}[{\text{kJ}}/{\text{mol}}]=53.88+\sum G_{{\text{form}},i}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/88f1922d8cfd2d9c88afdebe36584f9557636999)
Heat capacity (ideal gas)
![{\displaystyle C_{P}[{\text{J}}/({\text{mol}}\cdot {\text{K}})]=\sum a_{i}-37.93+\left[\sum b_{i}+0.210\right]T+\left[\sum c_{i}-3.91\cdot 10^{-4}\right]T^{2}+\left[\sum d_{i}+2.06\cdot 10^{-7}\right]T^{3}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5ae2f45d0ad4e1358033466231bedc7e4c6971b7)
Heat of vaporization at normal boiling point
![{\displaystyle \Delta H_{\text{vap}}[{\text{kJ}}/{\text{mol}}]=15.30+\sum H_{{\text{vap}},i}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/25c2ac235c1bd0109b3670a794306a1053466ac7)
Heat of fusion
![{\displaystyle \Delta H_{\text{fus}}[{\text{kJ}}/{\text{mol}}]=-0.88+\sum H_{{\text{fus}},i}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3885a8777dde47f4a1e7aa4e957e302380424d5e)
Liquid dynamic viscosity
![{\displaystyle \eta _{\text{L}}[{\text{Pa}}\cdot {\text{s}}]=M_{\text{w}}exp{\left[\left(\sum \eta _{a}-597.82\right)/T+\sum \eta _{b}-11.202\right]},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/dc922223e7bf93e11d34cbd9caa9d50ba7f0b846)
[3. Joback法計算Webアプリ]

原子団の加算値が揃っていればJoback法で定義されている物性値は計算することができる。それでは、加算値の求まっていない原子団や新たな原子団の加算値を決めるのはどうしたらいいだろうか?
[4. JOBACK法拡張]
山本は代替フロンの設計に拡張Joback法を検討した。
例えばCF3のパラメータを決めたいとする。
CF3CH2CH3の沸点の実験値は260.15Kになる。
Tb=260.15=198.2 + fCF3*1+ fCH2*1+ fCH3*1=198.2 + fCF3*1+ 22.88*1+23.58*1
fCF3は決まる。
(実際には多数のデータから統計的に決める)
沸点の加算値の拡張[*1]
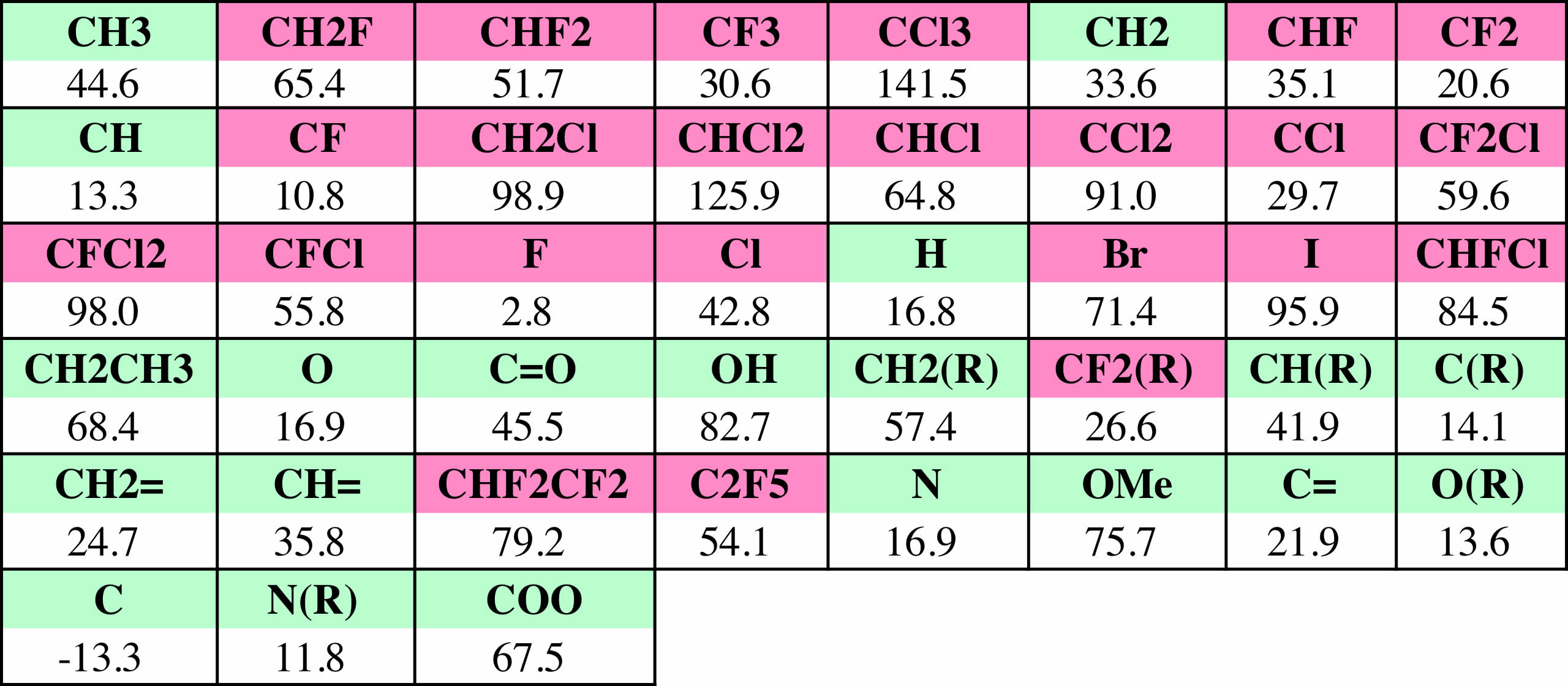
臨界点の加算値の拡張[*2]
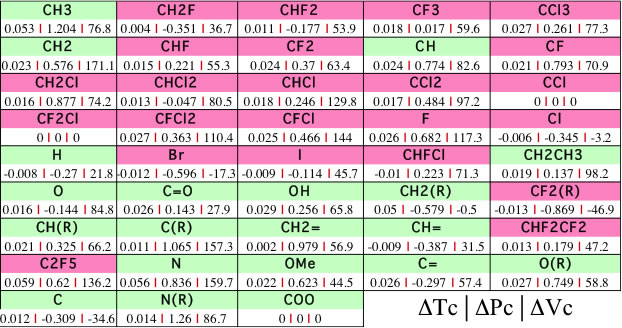
JOBACKの係数を活かす場合と、代替フロン専用に新しく構築する場合がある。パラメータの作成にLASSDGE法[*3]を適用することも大事になる、
[5. Pirikaのリンク]
*1 沸点の加算値の拡張
*2 臨界点の加算値の拡張
*3 LASSDGE法
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください。
