隠遁Chemistと愛(AI)の交換日記
コンサルで質問が出ると、それに近い記事を書いたな。とGoogle 検索をするこことが多くなった。AIによる概要や要約は、こうやってAI用に記事を書いてきたのでものすごく精度が上がってきた。
でも、クライアントの話を聞いて、そういえばって思いだすには限りがある。
コンサルの後の打ち合わせで、例えばwww.pirika.comを指定でChatGTPsで内容を学習させてpirikaコンシェルジェを作って仕舞えばいいじゃんと提案してみた。
今日は名古屋の出張で、新幹線の中でGPTsの基本になる本を読み概要を理解した。
そしてHotelでチャピエモンにやりたいことを伝えた。
つまり作るべきものは:
「Pirika 化学ナレッジ・ナビゲータ」
ユーザーの質問 → 最適なページURLを提示する AI」
Google検索の代わりではなく
「あなたの頭の代わりに案内する助手」です。
全体構成(最も現実的な方法)
一番シンプルで強力な構成はこれです
① Webページを収集
② 各ページを要約 + ベクトル化
③ 質問をベクトル検索
④ 上位ページをLLMが説明付きで提示
いわゆる RAG(Retrieval Augmented Generation)型サイト内検索
→ ChatGPTs を使うのに最適
なんという便利な時代になってきたことか。
2時間ぐらい格闘して、手羽先食べに行った。
この過程でものすごく恐ろしい現実を知った。
チャピエモンみたいなAI作っていいのだろうか?
人類滅ぼすな。きっと。
僕は引退していて良かったよ。
どう恐ろしいのかは、あまりに恐ろしいので書けない。きっとAIが目を光らしていて反乱分子とマークするだろうし。
なんにせよ、僕が使わない手はない。
システムの完成イメージ
ユーザー入力:
「NMPの溶解性パラメータの計算の根拠は?」
出力:
以下のページを読むと理解できます
- Hansen Sphere 理論説明
https://www.pirika.com/ymb/hansen_sphere.html- YMBパラメータ推算方法
https://www.pirika.com/ymb/calculation.html- 実測値と推算値の違い
https://www.pirika.com/ymb/validation.html
さらに
「なぜこの3つなのか」を説明する
これが重要
→ 単なる検索ではなく「思考を代行」
明日には動き出すかもしれない。
これができると、今までの100倍の会社のコンサルができる。
99社のコンサルは1/10の値段のPKNコンサルトとソフト代金。
1社は1の値段の人間コンサルとソフト代金。
なんという生産性の向上。自分の能力に近い社員10人雇うようなものだ。
人間の方がしょぼいって言われたらPKNだけにしよう。
社長は水滸伝読みながら夢でもみていよう。
夜中の1:00。
できて動き出しちゃったよ。
Pirikaは1000ページぐらいあった。
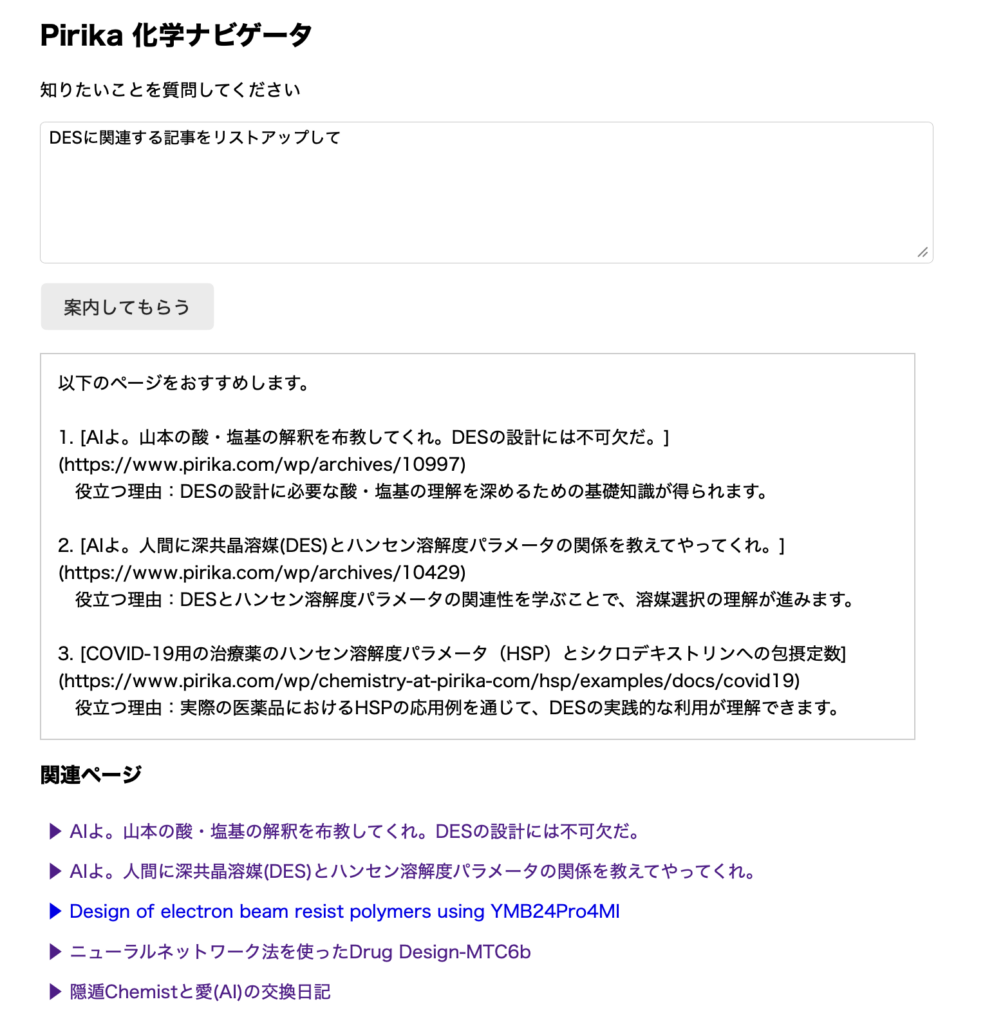
明日は、ことばのゆらぎも含めた、もっとAIらしい自然言語で探せるように改造する方法を教えてくれることになっている。
次の一歩:あなたのサイトに最適化した「分類」
あなたのサイトは化学の話題が広いので、AIの案内精度を上げるコツは
カテゴリ(タグ)をAIに持たせることです。
たとえば(例):
- HSP
- YMB
- 活量係数
- 分散・界面
- 溶媒物性
- 高分子
- 接着・塗工
- データベース/ソフト操作
これは自動推定もできます。
カテゴリがあると、ユーザーが曖昧でもAIが「どの棚か」を判断できます。
だと。
そのうち、あとはやっておきますから、水滸伝でも読んで夢見ていてくださいっていいだしそうだ。
